"Nếu có ai hỏi tôi rằng tôi sẽ bỏ phiếu cho ai đoạt giải
Nobel, tôi sẽ ưu tiên Karikó và Weissman" - Derrick Rossi, giáo sư Trường
Y Harvard, đồng sáng lập công ty công nghệ sinh học Moderna.
Khi Katalin Karikó
cùng chồng và con gái đặt bước chân đần tiên xuống nước Mỹ, trong tay họ gần
như chẳng có gì. Quy định người nhập cư khi đó chỉ được đổi tối đa 100 USD, cô
phải bàn với chồng bán chiếc xe hơi gia đình ở chợ đen, giấu số tiền đó vào gấu
bông của con gái. Và họ đã làm đúng như vậy.
Năm 1985, nhà hóa sinh
người Hungary quyết định rời quê hương để theo đuổi giấc mơ Mỹ, một giấc mơ
chung của cả một thế hệ người Đông Âu thời đó.
"Ở nhà, chúng tôi cũng vừa
chuyển đến một căn hộ mới. Con gái của chúng tôi mới được 2 tuổi, mọi thứ đang
rất tốt và chúng tôi rất hạnh phúc", Karikó ngậm ngùi nói. "Nhưng chúng tôi cũng phải đi thôi".
Phía bên kia Đại Tây Dương, nước Mỹ trong cơn khát chất xám đã hứa cho Karikó một vị trí nghiên cứu sau tiến sĩ tại Đại học Temple. Đó là tất cả những gì mà gia đình Karikó có thể bám víu vào. "Ngoài ra, chúng tôi không quen biết ai ở đây cả. Chuyến đi này chúng tôi chỉ có vé một chiều", cô nói.

Vậy là ngoài 100 USD tiền đổi cộng với 1.000 USD giấu được trong con gấu bông, thứ tài sản lớn nhất mà Karikó mang tới Mỹ khi đó chỉ còn khối chất xám trong đầu cô, nơi những ý tưởng về một công nghệ sinh học hoàn toàn mới đang được thai nghén: vắc-xin mRNA.
Trong thế giới tự nhiên, cơ thể chúng ta phải
dựa vào hàng tỷ protein siêu nhỏ để duy trì sự sống và sức khỏe.
Enzyme có
trong nước bọt đang giúp bạn tiêu hóa thức ăn là một loại protein. Hemoglobin
trong máu đang giúp vận chuyển oxy tới từng tế bào của bạn cũng là protein. Tất
cả các kháng thể của hệ miễn dịch đang giúp bạn chống lại mầm bệnh cũng là
protein.
Protein xây
dựng lên tóc, cơ bắp và cả xương của bạn. Chính xác thì protein có mặt và làm
nên từng tế bào trên cơ thể chúng ta. Nhưng cái gì tạo nên protein?
Quá trình
sinh tổng hợp của protein trong tế bào đã được nghiên cứu từ những năm 1940.
Trong đó, các nhà khoa học biết chúng được tạo thành từ các mảnh nhỏ hơn được
gọi là axit amin. Axit amin lại được cấu thành từ 4 nguyên tố của sự sống bao
gồm Carbon (C), Hydro (H), Nitơ (N) và Oxy (O).
Cơ thể con người chỉ có tổng cộng 20 axit amin, nhưng sự sắp xếp của chúng có thể tạo ra từ 80.000 -400.000 protein. Quá trình sắp xếp axit amin được thực hiện ở ribosome của tế bào, trong một động tác được gọi là dịch mã.
Đầu vào của quá trình dịch mã tạo ra protein
này chính là các mRNA hay RNA thông tin. mRNA có nhiệm vụ nói cho tế bào biết
loại protein nào mà nó đang thiếu. Sau khi nhận được thông tin từ mRNA, tế bào
mới chỉ đạo sản xuất ra đủ lượng và loại protein mà nó cần để hoạt động.
Về lý
thuyết, nếu bạn có thể thiết kế ra một loại mRNA của riêng mình và đưa vào tế
bào, bạn có thể chiếm quyền điều khiển quá trình dịch mã và tạo ra bất kỳ loại
protein nào bạn muốn – từ kháng nguyên để chủng ngừa bệnh truyền nhiễm, các
enzym để đảo ngược một căn bệnh hiếm gặp hoặc các tác nhân tăng trưởng để hàn
gắn các mô tim bị tổn thương.
Trong nhiều thập kỷ, các nhà khoa học đã mơ về khả năng dường như vô tận của mRNA. Họ coi nó như một cuốn sách công thức cho hàng nghìn tỷ tế bào của cơ thể. Ý tưởng là nếu bạn có thể tổng hợp ra một mRNA nhân tạo và tiêm nó vào cơ thể mình, mỗi tế bào trong cơ thể bạn sau đó cũng sẽ đều trở thành một nhà máy sản xuất thuốc hoặc vắc-xin theo yêu cầu.
Với công nghệ vắc-xin mRNA, bạn có thể miễn
nhiễm với căn bệnh mà không cần phải tiêm vào cơ thể phiên bản virus được làm
yếu. Và cũng bởi vậy, vắc-xin mRNA an toàn hơn rất nhiều so với vắc-xin truyền
thống, bạn không thể vô tình bị nhiễm bệnh từ chúng.
Công nghệ mRNA chính là thứ đã giúp chúng ta có được những liều vắc-xin COVID-19 đầu tiên trong đại dịch năm 2020. Nhưng trở lại thập niên 1980, đó vẫn là một câu chuyện hoàn toàn viễn tưởng.
Đơn xin tài trợ liệu pháp mRNA đầu tiên của
Karikó đã bị từ chối vào năm 1990, một năm sau khi cô chuyển công tác đến Đại
học Pennsylvania. Sau đó, hết lần này đến lần khác chúng còn bị từ chối nhiều
hơn nữa.
"Tôi tiếp tục viết và cải thiện cách tiếp cận – thiết kế ra những
RNA tốt hơn, phân phối tốt hơn", Karikó nói. "Tôi đã đưa ra các ứng dụng, v.v., cố gắng xin tài trợ của chính
phủ, tài trợ tư nhân từ các nhà đầu tư, nhưng mọi người đều từ chối".
Vấn đề nằm ở một điểm chí tử của công nghệ mRNA. Những phân tử này là thứ mà hệ miễn dịch sẽ nhận diện như một mầm bệnh ngoại lai, và sẽ tiêu diệt chúng trước khi mRNA có thể kích hoạt tế bào sản xuất ra protein cũng như vắc-xin.
Đó là lý do tới năm 1990, các nhà khoa học Mỹ
bắt đầu hoài nghi về mRNA. Họ nhận thấy RNA trần khi được tiêm vào cơ thể người
sẽ gây ra phản ứng miễn dịch cấp tính. Phản ứng này sẽ gây viêm tại chỗ và phá
hủy toàn bộ mRNA được tiêm vào trước khi chúng tiếp cận được tế bào, chứ chưa
nói đến đoạn kích hoạt nhà máy ribosome để sinh ra protein như mong muốn.
Những mũi
tiêm mRNA bị đánh giá là hoàn toàn vô nghĩa, sẽ chẳng có nhà máy vắc-xin nào
trong cơ thể, và chẳng có protein nào được tạo ra cả. Karikó đã mất 6 năm để
giải bài toán hóc búa mà cô gặp phải. Nhưng không có tài trợ đồng nghĩa với
việc bài toán ấy sẽ trở thành một nghịch lý:
Khi liệu
pháp mRNA không nhận được sự tin tưởng, sẽ không có ai tài trợ cho dự án phát
triển chúng. Khi không có ai tài trợ cho các dự án mRNA, công việc nghiên cứu
chúng sẽ bị đình trệ. Và khi nghiên cứu bị đình trệ thì đột phá sẽ không được
tạo ra. Mọi người sẽ tiếp tục không tin vào tiềm năng của mRNA.
Vòng luẩn quẩn ấy cứ lặp đi lặp lại, sẽ không có ai tài trợ cho Karikó và công nghệ mRNA sẽ vĩnh viễn bị chôn vùi.
Karikó bị giáng chức tại Đại học Pennsylvania
vào năm 1995, bởi công trình nghiên cứu của cô bị đánh giá là dậm chân tại chỗ.
Đó là một hình thức kỷ luật thường sẽ kết thúc sự nghiệp khoa học của những nhà
nghiên cứu thời đó.
Lương giảm,
không thu hút được sinh viên, Karikó thậm chí còn mới mắc ung thư và chồng cô
thì bị kẹt lại Hungary sau một chuyến trở về rồi không xin lại được visa vào
Mỹ.
"Bất cứ ai ở vào hoàn cảnh của tôi khi đó đều sẽ nghĩ đến chuyện buông xuôi. Mọi thứ ập đến quá kinh khủng", Karikó nói. "Tôi đã nghĩ đến chuyện trốn chạy tới một nơi khác, tìm một công việc khác. Tôi cũng tự dằn vặt và nghĩ rằng hay mình không đủ giỏi, không đủ thông minh".
"Tôi đứng bên cạnh chiếc Xerox và nói với anh ấy rằng tôi có thể
tạo ra bất cứ mRNA nào mà tôi mong muốn", Karikó nhớ lại. Đó là những gì mà cô
vẫn nỗ lực để đạt được trong 2 năm tiếp theo sau khi bị giáng chức và mất tiền
tài trợ nghiên cứu.
Mặc dù mắc
bệnh ung thư, Karikó vẫn cố gắng giữ cho ngày làm việc của cô bắt đầu lúc 6 giờ
sáng. Cô ấy lao đầu vào công việc ngay cả trong ngày cuối tuần và ngày lễ -
thậm chí thỉnh thoảng ngủ lại ban đêm trong văn phòng.
"Những người khác nhìn vào sẽ nghĩ tôi thật điên rồ và chật
vật, nhưng bản thân tôi thấy mình hạnh phúc khi ở trong phòng thí
nghiệm",
cô nói. "Chồng tôi ngày nào cũng nói "Khoa học cứ như trò giải
trí cho em vậy". Tôi đáp lại rằng: "Thì em đâu có đi làm
đâu. Đến phòng thí nghiệm giống như đi chơi hơn".
Trong những giờ khắc nản chí nhất của mình, Karikó đã nghĩ "dù thế nào mình cũng phải tiếp tục công việc".
Weissman hiểu tầm quan trọng của những gì
Karikó nói đồng thời bị cuốn hút bởi câu chuyện và niềm đam mê của cô với mRNA.
Cô ấy kể lần đầu tiên mình biết đến những phân tử kỳ diệu này là năm 1976, khi
còn là một cô sinh viên tại Đại học Szeded, Hungary.
Trước đó,
mRNA đã được tìm thấy vào năm 1961, một khám phá ngay lập tức đã gây ra một cơn
địa chấn trong giới khoa học mùa hè năm đó.
Với sự phát
hiện ra vai trò của phân tử này trong quá trình phiên mã từ DNA và dịch mã ra
protein, sau 10 năm trời, các nhà khoa học mới có thể chứng minh DNA không phải
là một chuỗi xoắn vô dụng trong tế bào, mà chính là thành phần quan trọng nhất
của nó.
Sau đó, họ
bắt đầu tự hỏi liệu có thể lợi dụng phân tử mRNA này để biến cơ thể chúng ta
thành nhà máy sản xuất thuốc và vắc-xin hay không? Hướng nghiên cứu này bị rơi
vào bế tắc trong suốt 14 năm, bởi khoa học thời điểm đó chỉ đơn thuần là không
có các thiết bị để chế tạo ra mRNA nhân tạo.
Các nhà khoa
học chỉ có thể chiết xuất mRNA từ tế bào, chứ không thể tạo ra các mRNA hoàn
toàn mới. Vậy thì khả năng thao túng tế bào và biến chúng thành các nhà máy sản
xuất vắc-xin cũng giống như chúng ta nhìn thấy một Hệ Mặt Trời mới bên ngoài vũ
trụ mà không có một chiếc tàu du hành nào bay được tới đó.
Nhưng đến
năm 1984, nhà hóa sinh người Mỹ Kary Mullis đã phát minh ra phản ứng chuỗi
polymerase (PCR), một phương pháp khuếch đại một lượng rất nhỏ DNA lên số lượng
lớn. Đó là tiền đề cho phép các nhà nghiên cứu có thể sử dụng PCR để tạo mRNA
nhân tạo vào năm 1989.
"Đối với các nhà khoa học làm việc trên mRNA, đó quả là một đột phá mạnh mẽ", Karikó nói. "Đột nhiên chúng tôi cảm thấy mình có thể làm được mọi thứ". Nhưng máy PCR chỉ mới phổ biến ở Mỹ khi đó, Karikó đã phải đưa ra một quyết định khó khăn, rời khỏi Hungary để theo đuổi giấc mơ của mình.
10 năm ở Mỹ sau đó là khoảng thời gian vừa đủ
cho giấc mơ Mỹ của Karikó bị sụp đổ. Làm việc tại Đại học Temple được 4 năm thì
Karikó gần như bị ép phải thôi việc sau một lần tranh cãi kịch liệt với sếp. Cô
chuyển sang Đại học Pennsylvania để tiếp tục nghiên cứu thì lại đụng phải một
hòn đá tảng thứ hai trong lĩnh vực mRNA.
Đó là việc
không còn ai có thể tin họ có thể phân phối mRNA vào bên trong cơ thể người mà
không tạo ra phản ứng miễn dịch khiến mũi tiêm trở nên vô dụng, thậm chí gây
nguy hiểm cho người nhận chúng. Karikó đã làm hàng ngàn chồng hồ sơ xin tài
trợ, thuyết trình khắp mọi nơi để thuyết phục những ai có thể tin vào điều đó
nhưng cô đã thất bại.
Vậy mà chỉ một cuộc nói chuyện tình cờ ngắn ngủ bên cạnh máy photocopy, cô ấy lại vô tình thuyết phục được Weissman- người tuy chỉ là đồng nghiệp mới của cô nhưng lại đang nắm trong tay đủ nguồn lực để hỗ trợ Karikó tiếp tục giấc mơ của mình.
Biết được Karikó hiện
đang khó khăn trong việc xin tài trợ, Weissman đã chia sẻ một phần tiền trong
phòng thí nghiệm của anh sang cho cô. "Điều ấy đã giúp tôi thấy lạc
quan hơn để tiết tục", Karikó nói. "Mặc dù lương của tôi được trả
còn thấp hơn cả kỹ thuật viên trong phòng của Drew, nhưng sự ủng hộ của anh ấy
đã khiến tôi tập trung để vượt qua những trở ngại".
Không chỉ tài trợ kinh phí, Weissman còn trực tiếp tham gia vào cùng với Karikó trong việc giải nút thắt cho bài toán phân phối mRNA. Họ để ý các nghiên cứu trước đó cho thấy hệ miễn dịch của vi khuẩn có thể được kích hoạt để chống lại virus xâm nhập nhờ vào các dấu hiệu đặc trưng trên nucleotide cấu thành RNA virus.
Mỗi chủng virus dường như đều có các dấu vết
đặc trưng trên nucleotide của mình - bao gồm adenine (A), cytosine (C), guanine
(G) và uracil (U) - giống như một dấu vân tay của con người. Một khi vi khuẩn
nhận ra dấu "vân tay lạ", chúng sẽ kích hoạt hệ thống miễn dịch để
tiêu diệt virus xâm nhập.
Karikó và
Weissman nghi ngờ rằng hệ miễn dịch của con người cũng đã hoạt động theo cơ chế
tương tự. Và nếu họ có thể đánh lừa được nó, mRNA sẽ có thể được tiêm vào cơ
thể một cách an toàn mà không gây ra phản ứng miễn dịch nguy hiểm.
Nhưng
làm thế nào để đánh lừa cơ thể? Karikó và Weissman đã liên tục biến đổi các
nucleotide này thành một phân tử "nhân tạo" thay
thế cho chúng.
Ví
dụ, biến adenine A thành A’, A’’, A’’’… Các phân tử A’ này về cơ bản vẫn là
adenine A, làm nhiệm vụ như một adenine A trong quá trình phiên mã và dịch mã,
đảm bảo chức năng tạo ra protein. Nhưng chúng sẽ có các "dấu vân tay" khác nhau, và một trong số đó là
dấu vân mà hệ miễn dịch của cơ thể người không nhận được ra.
Đầu những
năm 2000, Karikó tình cờ phát hiện ra một thay đổi trên uracil (U) chính là thứ
mà cô đang tìm kiếm. Một sửa đổi trên nucleotide này biến U thành U’ đã
ngăn chặn được phản ứng miễn dịch trên chuột khi được tiêm mRNA ngoại lai.
"Tôi đã nhớ Drew khi đó đã phải thốt lên: Ôi trời, nó không gây ra phản ứng miễn dịch này!", Karikó nói. "Tại thời điểm đó, chúng tôi đã biết đây là một cột mốc rất quan trọng, vì nó có thể mở ra con đường dẫn tới các liệu pháp y tế và vắc-xin mới".
Đó là năm 2005, Karikó và Weissman đã xuất bản
một bài báo, nộp một bằng sáng chế và thành lập một công ty công nghệ sinh học
để thương mại hóa sản phẩm của mình. Nhưng rốt cuộc, cả cộng đồng khoa học hầu
như chẳng ai quan tâm đến sáng chế mới của họ.
"Không ai mời chúng tôi đi bất cứ đâu để nói về nó", Karikó nhớ lại.
Đại học Pennsylvania đã thẳng tay bán bằng sáng chế độc quyền của Karikó và
Weissman cho bên thứ ba.
Bẵng đi một
thời gian năm 2010, khi Derrick Rossi, một giáo sư tại Trường Y Harvard đọc được
nghiên cứu 5 năm trước của Karikó. Ngay lập tức, Rossi đã nhận ra đó là một
công trình xứng đáng với một giải Nobel.
"Nếu có ai hỏi tôi rằng tôi sẽ bỏ phiếu cho ai, tôi sẽ ưu tiên
Karikó và Weissman. Khám phá cơ bản của họ cuối cùng sẽ trở thành những loại
thuốc giúp ích cho thế giới", ông nói.
Tầm nhìn của
Rossi được hiện thực hóa vào cùng năm đó, ông đã cùng với một nhóm giáo sư
Harvad và MIT lập ra Moderna, một công ty công nghệ sinh học nhắm đến việc sửa
đổi mRNA để tạo ra vắc-xin và thuốc điều trị bệnh.
Đại diện của Moderna cũng đã tiếp cận với Karikó và Weissman để mua bằng sáng chế sửa đổi mRNA của cặp đôi, nhưng đã quá muộn, Đại học Pennsylvania trước đó đã bán nó cho một công ty khác là Cellscript.
Moderna vì thế phải tự mình nghiên cứu tạo ra các
bản sửa đổi mRNA mới, nhưng về cơ bản, công việc của họ vẫn dựa trên những khám
phá của Karikó và Weissman. Quá trình lặp lại đó mất tới 4 năm, Moderna cuối
cùng cũng đạt tới những thành công nhất định.
Năm 2013, nghiên cứu của họ đã thu hút được AstraZeneca, gã dược phẩm khổng lồ của Anh đang tìm kiếm những đột phá mới trong ngành dược. Họ đã quyết định đầu tư 240 triệu USD vào Moderna để tìm kiếm, phát triển và thương mại hóa các phương pháp điều trị mRNA cho các bệnh liên quan đến tim mạch và ung thư.
Cùng năm Moderna đạt được bước tiến ấy, Karikó
được mời tới Đức. Ở đó, có một doanh nhân gốc Thổ Nhĩ Kỳ tên là Ugur Sahin cũng
đã nhìn ra được sự phát triển của lĩnh vực nghiên cứu mRNA. Ông ấy đã thành lập
một công ty khởi nghiệp khác tên là BioNTech.
Tài năng của
Karikó lúc bấy giờ đã được giới đầu tư mạo hiểm đặc biệt chú ý, thậm chí tranh
giành nhau để có sự phục vụ của cô. Moderna cũng là một trong số những công ty
sẵn sàng trải thảm đỏ mời cô ấy đến làm việc. Nhưng Đại học Pennsylvania thì
dường như vẫn tuyệt nhiên coi Karikó như một đứa con ghẻ.
Họ từ chối
đơn xin bổ nhiệm lại vị trí giáo sư mà cô ấy đã bị giáng chức từ năm 1995, lấy
lí do Karikó không có năng lực giảng dạy. Giọt nước tràn ly này đã khiến cô ấy
dứt áo ra đi. Karikó nhận lời Ugur Sahin để trở thành Phó chủ tịch cấp cao tại
BioNTech.
"Khi tôi nói với họ rằng tôi sẽ rời đi, họ đã cười nhạo tôi và nói rằng BioNTech chỉ là một công ty còn không có trang web", Karikó nhớ lại.
Tại BioNTech, Karikó đã lãnh đạo chương trình
nghiên cứu phương pháp thay thế protein RNA để tạo ra các loại vắc-xin và thuốc
chữa bệnh mới. Năm 2017, họ đã đạt được tới thành công khi phát triển được một
vắc-xin mRNA đầu tiên chống lại được virus Zika trên chuột và khỉ.
Cùng năm đó,
Moderna cũng tạo ra được một vắc-xin chống lại Zika của riêng mình. Nhưng công
nghệ mRNA nhìn chung vẫn chỉ là một thứ gì đó nằm ngoài tầm radar của công
chúng và giới truyền thông, ngoại trừ những doanh nhân đứng đầu các quỹ mạo
hiểm muốn đầu tư vào đó.
Mọi chuyện
chỉ thay đổi vào năm 2019, sau khi một virus corona có tên là SARS-CoV-2 được
phát hiện tại Trung Quốc và gây ra đại dịch toàn cầu COVID-19 chỉ trong vòng 1
năm sau đó. Cả Moderna và BioNTech đều biết rằng đây chính là cơ hội để chứng
minh bản thân mình với thế giới.
Với tất cả
kinh nghiệm trong lĩnh vực này, Moderna chỉ mất 2 ngày sau khi gộ gen
SARS-CoV-2 được giải mã để thiết kế ra một loại vắc-xin chống lại COVID-19.
Cùng khoảng thời gian đó, Karikó và BioNTech ở Đức cũng đã khởi động một chương
trình phát triển vắc-xin cho riêng mình hợp tác với gã dược phẩm khổng lồ Mỹ
Pfizer.
Tháng 11 năm
2020, những mũi vắc-xin COVID-19 đầu tiên của liên doanh Pfizer/BioNTech đã
được cấp phép tiêm chủng tại Anh, sau đó là Mỹ và hàng loạt quốc gia khác trên
thế giới. Thử nghiệm lâm sàng cho thấy vắc-xin dựa trên công nghệ mRNA mà
Pfizer/BioNTech phát triển có hiệu quả tới hơn 90%.
Liên doanh
đã hứa cung cấp hàng trăm triệu liều vắc-xin mRNA cho thế giới vào cuối năm
2021: 300 triệu liều được đặt hàng bởi Liên minh Châu Âu, 120 triệu liều từ
Nhật Bản, 100 triệu liều cho Mỹ và 40 triệu liều cho Vương quốc Anh.
Moderna cán đích thứ hai trong cuộc đua sản xuất vắc-xin COVID-19 với cùng công nghệ mRNA tương tự đã được ươm mầm từ nghiên cứu của Karikó từ hơn 20 năm về trước. Những thay đổi trong phân tử mRNA bé nhỏ đã biến Moderna từ một công ty khởi nghiệp thành một công ty có trị giá 35 tỷ USD, sau khi vắc-xin COVID-19 của họ kết thúc thử nghiệm lâm sàng với hiệu quả 94%.
Phía bên kia Đại Tây Dương, BioNTech cũng từ một công ty khởi
nghiệp "chẳng có nổi một trang web" đã trở
thành một công ty trị giá 25 tỷ USD với hơn 1.500 nhân viên. Karikó, hiện đã 65
tuổi, vẫn đang giữ vị trí Phó chủ tịch cấp cao tại BioNTech.
Ngày cô rời nước Mỹ về Châu Âu, Karikó đã nói với chồng mình
rằng: "Em sẽ không về cho đến ngày mũi
vắc-xin mRNA được tiêm cho người đầu tiên. Anh biết đấy, em có một khao khát
nhìn thấy người đầu tiên được chữa khỏi".
"Bây giờ thì tôi có thể về nhà
được rồi",
Karikó nói.
Những mũi tiêm vắc-xin
COVID-19 của Pfizer/BioNTech đã được tiêm cho 40.000 người thử nghiệm vào tháng
11 năm 2020. 50 triệu liều vắc-xin của họ đã được chốt đơn hàng vào cuối năm
ngoái. Dự kiến đến chỉ trong vòng năm 2021, Pfizer/BioNTech sẽ sản xuất và phân
phối hơn 1,3 tỷ liều vắc-xin COVID-19 cho toàn thế giới.
Sau tất cả những nghịch cảnh mà mình trải qua để đi tới thành
công, Karikó chỉ chia sẻ một động lực giữ cho cô ấy trở nên lạc
quan: "Tôi luôn tâm niệm rằng mình cần
phải giúp đỡ mọi người, vì vậy, tôi đã luôn cố gắng để đưa các nghiên cứu của
mình trở thành những ứng dụng ngoài đời thực".
Nhưng có lẽ chính bản thân Karikó cũng chưa bao giờ nghĩ mình có
thể giúp được nhiều người đến thế trong một dịch bệnh toàn cầu như COVID-19.
"Thực sự thì tôi chưa bao giờ tưởng tượng được
điều ấy sẽ xảy ra. Tôi chỉ cảm thấy rất vui khi đã đóng góp được một phần công
sức nhỏ bé của mình vào câu chuyện thành công này".
Bài viết:
Thanh Long
Thiết kế:
TOM
Ảnh:
Sưu tầm


















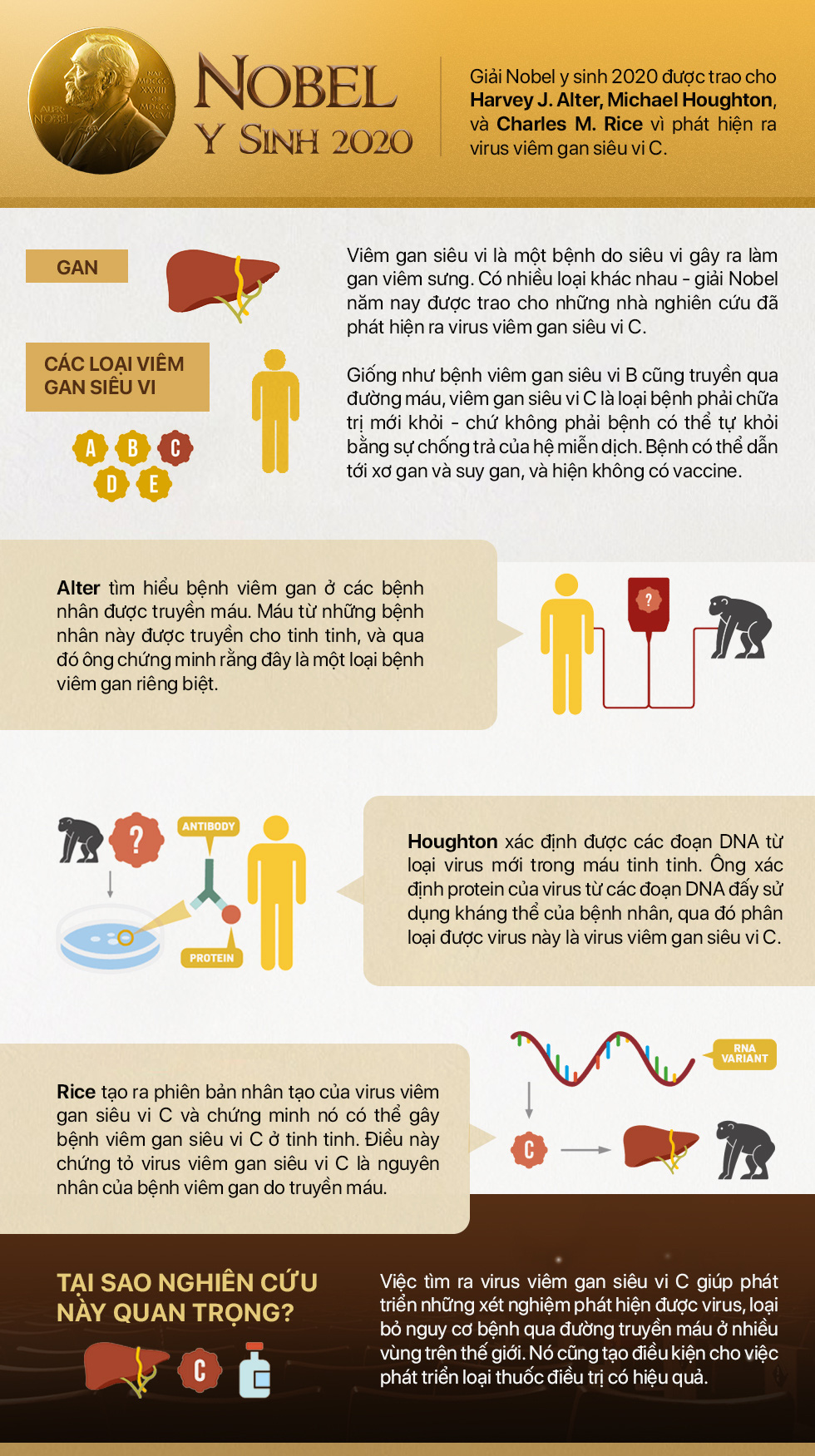
 TTO - Thời điểm công bố đã bị lùi lại chút ít nhưng rồi thì 3 nhà khoa học Roger Penrose, Reinhard Genzel và Andrea Ghez đã được xướng tên cùng nhận giải Nobel vật lý 2020 vì các công trình nghiên cứu hố đen vũ trụ.
TTO - Thời điểm công bố đã bị lùi lại chút ít nhưng rồi thì 3 nhà khoa học Roger Penrose, Reinhard Genzel và Andrea Ghez đã được xướng tên cùng nhận giải Nobel vật lý 2020 vì các công trình nghiên cứu hố đen vũ trụ.